中科院植入式腦機介面大突破:自動變形 貼附於大腦核心
11月4日消息,中國科學院上海微系統與資訊技術研究所研究團隊近日在《自然-通訊》發表重大成果,成功開發出蠶絲蛋白賦能的微創植入式柔性神經介面。
其“自動變形貼附大腦核心”的特性,一舉攻克深腦區監測的技術瓶頸,為帕金森病、阿爾茨海默病等神經疾病的診療開闢新路徑。
此前,深腦監測面臨“微創與精准”的兩難:穿刺式電極雖能抵達深部核團,卻易損傷腦組織且難以長期穩定監測;柔性平面電極雖貼附性好,卻無法微創植入大腦“內表面”。
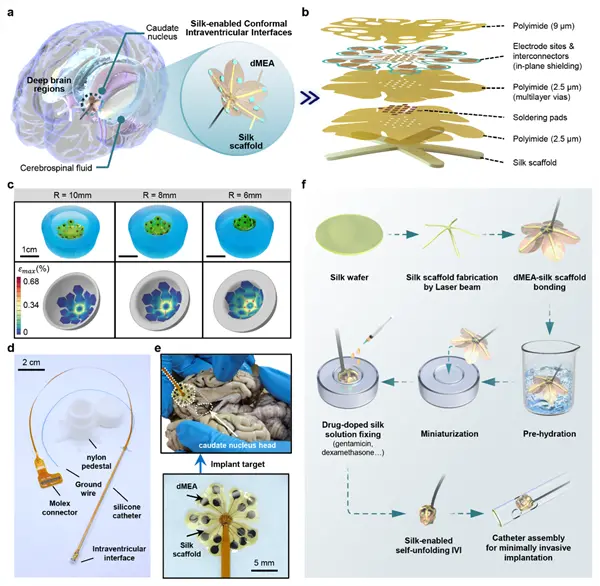
中科院團隊的創新方案完美破解這一矛盾——將形狀記憶絲蛋白支架與可變形微電極陣列結合,器件可微型化裝入臨床常用微創手術導管,實現微創遞送。
進入大腦側腦室後,絲蛋白支架在腦脊液環境中觸發形狀記憶功能,自動展開並精准貼附於尾狀核頭、腦室壁等深腦核心區域,如同為大腦“定制貼膜”。
電極走線層的共面金屬遮罩設計,能有效抑制工頻雜訊,確保信號採集的高信噪比,解決了動態腦脊液環境下的監測難題。
在“帕金森綿羊”模型的驗證中,該神經介面展現出卓越性能:不僅穩定捕捉到帕金森病特徵性β振盪信號,還能精准記錄左旋多巴藥物干預後的神經回應變化。
更關鍵的是,其在長達四周的慢性監測中,始終保持良好電學性能與組織相容性,為長期臨床應用奠定基礎。
這一突破填補了深腦區微創廣覆蓋監測的技術空白,為深腦核團相關神經疾病的解析提供了一種全新的技術手段。
來源:中國快科技



 您當前的位置 :
您當前的位置 : 










