
12月23日,Frontera Therapeutics(中文名稱:芳拓生物)遞表港交所,瑞銀集團、國泰海通擔任聯席保薦人。
招股書顯示,芳拓生物成立於2019年,專注於自主開發創新的重組腺相關病毒(rAAV)基因療法、目前,公司產品管線包括8款自主開發的rAAV基因治療候選藥物。如果順利上市,芳拓生物或有望成為“AAV基因治療第一股”。

芳拓生物產品管線
AAV作為一種複製缺陷型病毒的發現可追溯至1965年,基因治療的概念於1971年提出,而rAAV於1974年首次被用作基因遞送載體。FDA於1990年批准全球首項基因治療人體臨床試驗。2017年,Luxturna成為首款獲FDA批准的rAAV基因療法。2022年以來,受底層技術的成熟及更完善的監管框架所推動,基因治療藥物的批准率大幅加快。
FT-002是芳拓生物的核心管線之一,這是一種正在研究用於治療X連鎖視網膜色素變性(XLRP)的潛在全球同類最佳候選藥物。FT-003是一款潛在全球同類最佳候選藥物,正在研究用於透過玻璃體內注射治療新生血管性老年性黃斑病變(nAMD)及糖尿病黃斑水腫(DME)。招股書顯示,兩款藥物在中國的二期臨床招募完成,其中FT-003的nAMD適應證於2026年第三季度前開始中國三期臨床試驗。
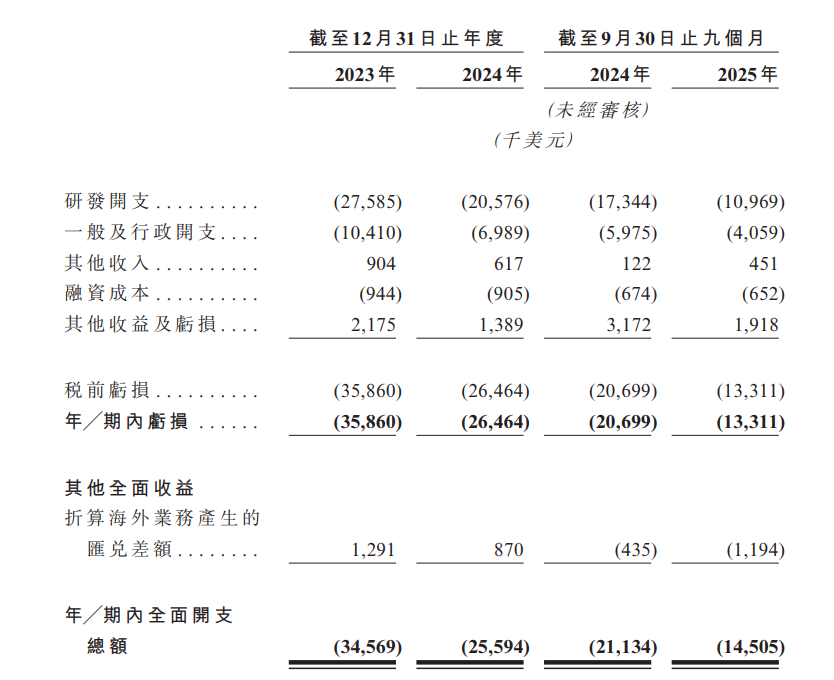
芳拓生物業績表現
目前,芳拓生物還沒有商業化產品。業績方面,截至2023年及2024年12月31日止年度,公司期內虧損分別為3590萬美元、2650萬美元,2025年前九個月錄得虧損1330萬美元。此次港股募資擬用於兩款核心產品的持續臨床研發活動,以及早期管線專案的研發等。
2015年以來,美國批准了16款基因治療藥物。2025年4月1日,國內首款基因療法才正式獲批,用於中重度血友病B(先天性凝血因數IX缺乏症)成年患者的治療,背後的公司是信念醫藥。由於基因療法往往針對的是超罕見疾病,所以其價格高昂。例如Luxturna是美國及歐洲批准用於治療RPE65介導IRD的唯一基因療法,每次治療的定價約為85萬美元。有公開資料稱,信念醫藥的單支價格達到9.3萬元,一個成人患者完整治療的總價超過400萬元。
高昂的價格也成為影響基因療法商業化的重要因素。芳拓生物在招股書的風險因素中提到,基因療法屬一種新型療法,且處於相對較早的商業化階段。考慮到與基因療法相關的高昂研發成本、複雜的生產工藝及專業的技術要求,基因療法產品的價格通常高於其他治療方案。倘公司候選藥物的治療成本相對於保險公司、其他第三方付款人、醫生及患者的支付意願而言過高,產品的市場接納度可能會受到嚴重限制。公司的部分候選藥物也採用了操作門檻相對較高的注射方法,此舉可能在商業化期間限制合資格醫院或機構的數目。資質不足及合作範圍受限可能令候選藥物無法迅速觸及廣泛的患者,並進一步對其商業化及市場接納度產生不利影響。
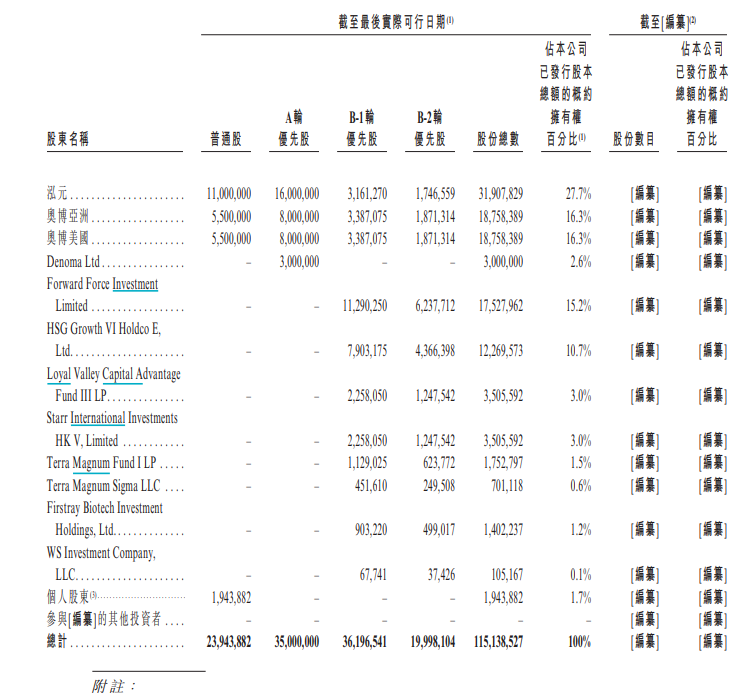
芳拓生物股東架構
股東方面,奧博資本實體及泓元為公司的創始股東。自註冊成立以來,公司一直由獨立於創始股東的管理團隊運營。招股書顯示,截至最後實際可行日期,泓元持有27.7%的股權,為最大單一股東。
芳拓生物的董事會共有9名董事組成,其中執行董事60歲的李新燕擔任首席執行官兼首席醫學官,也是公司的聯合創始人。招股書顯示,李新燕擁有5年臨床實踐經驗,以及超10年免疫學及生物技術研發經驗,並投身創新型藥物研發超過20年。李新燕曾在上海澤生科技開發股份有限公司、昆藥集團股份有限公司、科濟藥業控股有限公司全資子公司愷興生命科技(上海)有限公司等藥企工作。
來源:中國澎湃新聞
- 相關推荐
-
-
 漢堡王和波佩斯餐飲連鎖店的加盟商雷克斯概念公司計畫在華沙進行首次公開募股链接阅读
漢堡王和波佩斯餐飲連鎖店的加盟商雷克斯概念公司計畫在華沙進行首次公開募股链接阅读 -
 大眾與 Uber 在洛杉磯啟動自動駕駛巴士路測,所用車型為 ID.Buzz链接阅读
大眾與 Uber 在洛杉磯啟動自動駕駛巴士路測,所用車型為 ID.Buzz链接阅读 -
 地平線地瓜機器人再獲1.5億美元投資,B輪累計融資2.7億美元链接阅读
地平線地瓜機器人再獲1.5億美元投資,B輪累計融資2.7億美元链接阅读 -
 開年首季賺超去年全年的2倍!天華新能一季度淨利同比增超275倍链接阅读
開年首季賺超去年全年的2倍!天華新能一季度淨利同比增超275倍链接阅读 -
 星巴克中國:加速覆蓋空白城市,計畫未來三年將覆蓋至1500個縣級以上行政區链接阅读
星巴克中國:加速覆蓋空白城市,計畫未來三年將覆蓋至1500個縣級以上行政區链接阅读 -
 看好中國“十五五”核電增量,德國凱士比想拿下更高的核主泵市占率链接阅读
看好中國“十五五”核電增量,德國凱士比想拿下更高的核主泵市占率链接阅读 -
 穀歌大單拉動博通股價漲超6%,機構目標價上看500美元链接阅读
穀歌大單拉動博通股價漲超6%,機構目標價上看500美元链接阅读 -
 海光資訊一季度營收增長68%,去年淨利25億元增三成链接阅读
海光資訊一季度營收增長68%,去年淨利25億元增三成链接阅读
-









 您當前的位置 :
您當前的位置 : 




